Por Nsikan Akapan
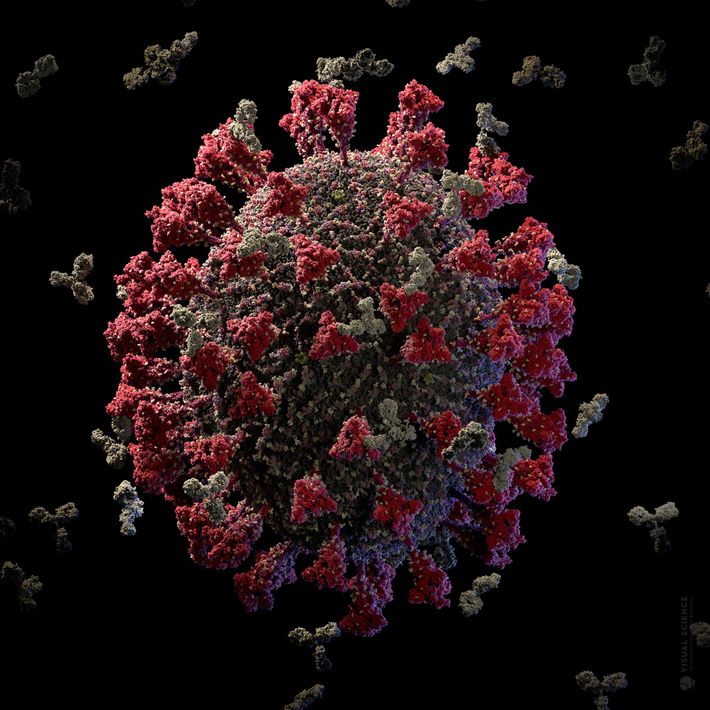
Um candidato promissor à vacina contra o coronavírus superou um obstáculo importante na última semana, quando a Moderna Therapeutics entrou na fase dois dos estudos clínicos. A conquista sinaliza que a vacina à base de RNAm da empresa foi aprovada nas verificações iniciais de segurança e alcançou um marco importante ao aproximar o medicamento dos mercados público e comercial.
Após quase cinco meses de mortes e paralisações econômicas provocadas pela pandemia da covid-19 em todo o mundo, as pessoas aguardam ansiosamente por algum sinal de esperança para que possam retornar à vida como era antes. Isso explica, em parte, a recente agitação envolvendo os resultados da Moderna e seu mais avançado candidato, que saiu do laboratório da empresa em Cambridge, Massachusetts, para estudos em humanos em um tempo recorde de 63 dias.
Em 18 de maio, a empresa de biotecnologia anunciou descobertas preliminares de que indivíduos saudáveis haviam respondido à sua vacina de RNAm produzindo “anticorpos neutralizantes”. Os anticorpos são as principais sentinelas produzidas pelo sistema imunológico para prevenir infecção pelo coronavírus. Especialistas foram rápidos em apontar que os resultados se referem a apenas oito pessoas de um total de 45 que participam do estudo, que está sendo conduzido pelo Instituto Nacional de Alergia e Doenças Infecciosas dos Estados Unidos. A empresa não divulgou informações suficientes para avaliar se os participantes da primeira fase apresentaram respostas imunes protetoras, que, de acordo com imunologistas, envolvem mais do que a simples produção de anticorpos.

Mas os detalhes apresentados pela Moderna, combinados com o último comunicado, sugerem que a empresa esteja caminhando para alcançar algo sem precedentes: licenciar a primeira vacina com tecnologia RNAm para uso humano.
“Os resultados são empolgantes porque possuem dados da primeira fase que demonstram que a vacina é segura, o que é muito importante”, diz Ali Salem, desenvolvedor de medicamentos e professor da Faculdade de Farmácia da Universidade de Iowa, que não participou do estudo da Moderna.
O estudo de fase dois envolverá cerca de 600 participantes de 10 centros e oito estados. Os centros recrutaram participantes e, se forem elegíveis com base nos exames físicos realizados, alguns receberão imunizações. A Moderna confirmou por meio de um comunicado à imprensa que os primeiros participantes em cada faixa etária do estudo — adultos abaixo e acima dos 55 anos — receberam doses do candidato desenvolvido pela empresa.
“Nossos investigadores principais diriam facilmente que esses estudos são os mais importantes que já realizaram na vida”, afirma Jaime Farra, diretor de marketing da Alliance for Multispecialty Research, que opera um centro do estudo em Newton, Kansas.
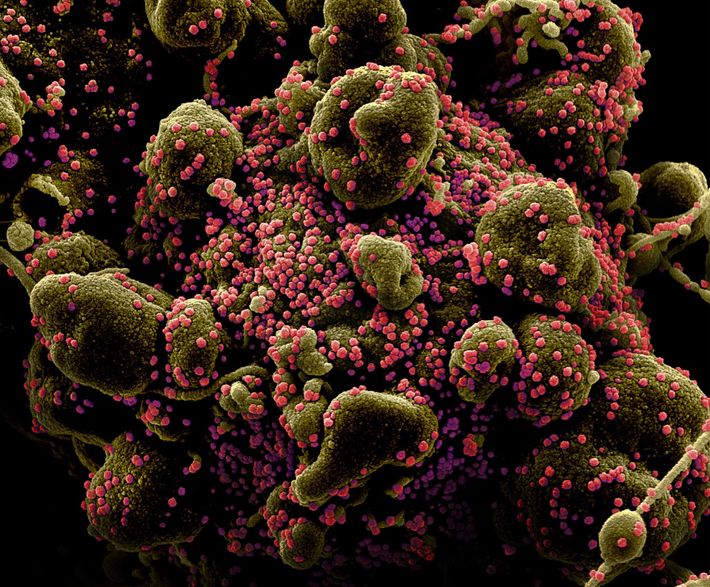
FOTO DE COLORIZED SCANNING ELECTRON MICROGRAPH BY NATIONAL INSTITUTE OF ALLERGY AND INFECTIOUS DISEASES, NIH
Como surgiram as vacinas de RNAm
Sempre que um micro-organismo infecta o corpo, nosso sistema imunológico se esforça para reconhecê-lo e formular um plano de resposta. As vacinas tradicionais utilizam essa resposta por meio da introdução, em nosso organismo, de vírus inteiros, porém inativos, ou de suas proteínas inteiras, desencadeando uma reação imune. Essas vacinas levam tempo para serem desenvolvidas, em parte porque os cientistas precisam cultivar e inativar o micro-organismo todo ou suas proteínas, e fazem isso de forma bem específica.
O RNA mensageiro é um material genético feito de ácido nucleico — o mesmo material que o nosso DNA — que percorre nossas células, dando instruções finais sobre quais proteínas construir para formar a arquitetura celular do corpo. No início da década de 1990, os cientistas se perguntaram o que aconteceria se produzissem pedaços de DNA viral e RNAm e os injetassem em células humanas ou animais de laboratório. A esperança era que as células captassem os fragmentos genéticos, produzissem proteínas virais e acionassem uma resposta imune.
Na teoria, esse método permitiria aos cientistas acelerar as vacinas; em vez de semanas, um candidato poderia ficar pronto para testes em horas ou dias. Esses candidatos à vacina também seriam mais flexíveis e duráveis contra vírus que tendem a evoluir por meio de mutações, como o coronavírus, influenza e HIV. Isso pode ajudar no desenvolvimento de uma vacina universal que seja eficaz contra várias cepas de um vírus, afirma Margaret Liu, presidente do conselho da Sociedade Internacional de Vacinas.
Trinta anos atrás, Liu estava entre o primeiro grupo de pesquisadores de laboratório a tentar utilizar vacinas de DNA e RNAm; seus primeiros resultados com uma vacina universal de DNA contra influenza foram os primeiros a demonstrar proteção e se mostraram os mais promissores — pelo menos em camundongos. Em geral, quando vacinas de DNA e RNAm foram produzidas pela primeira vez, elas demonstraram êxito sustentado em modelos animais, momento conhecido como estágio “pré-clínico” no desenvolvimento de medicamentos, mas as vacinas não produziram respostas imunes potentes em humanos.
“As pessoas pensaram que isso se devia ao fato dos humanos serem maiores”, conta Liu. Mas essa hipótese perdeu força após o desenvolvimento bem-sucedido de vacinas à base de DNA para cavalos, peixes e condores-da-califórnia.
Enquanto isso, as vacinas com tecnologia RNAm enfrentavam dificuldades, pois não eram estáveis. Uma vez dentro do corpo, o RNAm de uma vacina se decompõe mais rapidamente que o DNA, o que também limita a potência imune. Além disso, o RNAm pode intensificar as células imunes, causando reações adversas. Durante anos, esses desafios foram responsáveis por descartar as vacinas de RNAm e relegar as vacinas de DNA à medicina veterinária.
tória começou a mudar em 2005, quando cientistas da Universidade da Pensilvânia realizaram pequenas modificações químicas nas vacinas de RNAm. Essas modificações aumentaram a durabilidade e tornaram as vacinas mais seguras, causando menos respostas imunes adversas.
“Muitas pessoas começaram a considerar o RNAm como uma estratégia terapêutica para uma variedade de doenças”, diz Salem, da Universidade de Iowa. Uma delas seria a “ModeRNA Therapeutics”, agora conhecida como Moderna, empresa criada em 2010 depois que o pesquisador da Harvard Derrick Rossi usou RNAm modificado para reprogramar células-tronco em uma tentativa de tratar doenças cardiovasculares.
Ao longo dos anos, a empresa também passou a contar com uma famosa ferramenta para a administração de medicamentos chamada nanopartículas lipídicas. Ao preencher uma cápsula escorregadia feita de lipídios oleosos com material genético, essas partículas poderiam transportar o RNAm mais facilmente para dentro das células, onde ele poderia fazer o seu trabalho. Com tecnologia RNAm mais segura e melhor administração dos medicamentos, a empresa conseguiu expandir seu portfólio e buscar soluções para o câncer e diversas doenças infecciosas, incluindo a gripe. Mas o momento decisivo veio com o vírus zika transmitido por mosquitos.
Depois que o zika surgiu em 2015, os laboratórios se apressaram para encontrar uma vacina adequada. Justin Richner, agora professor assistente da Universidade de Illinois, em Chicago, fez parte de um projeto que envolveu diversas universidades que realizaram pesquisas iniciais sobre candidatos à vacina de RNAm desenvolvidos pela Moderna Therapeutics. Richner diz que a equipe aprimorou os códigos de RNAm, ação que levou uma das vacinas contra o zika da Moderna aos primeiros estudos em humanos em 2016 — momento em que o desenvolvimento se estagnou.

Segurança em primeiro lugar
A Moderna Therapeutics não respondeu aos diversos pedidos de entrevista da National Geographic. Mas as atualizações da empresa, que não são revisadas por pares, podem fornecer pistas sobre seu progresso na vacina contra a covid-19. Por exemplo, o anúncio feito pela Moderna em 18 de maio não apresentou números concretos sobre a quantidade de anticorpos detectados em humanos ou camundongos após a imunização. Mas revelou que a primeira fase de seu estudo sobre a covid-19 aparentemente alcançou seu objetivo principal de determinar a dosagem mais segura do medicamento.
“Quando se conduz um estudo clínico que nunca foi realizado em humanos antes, a informação mais importante a ser obtida é se a vacina é segura”, diz Maria Elena Bottazzi, reitora da Escola Nacional de Medicina Tropical da Baylor College of Medicine, que não participou do estudo da Moderna.
Ela acrescenta que um sinal mais concreto de êxito para a Moderna pode ser algum ponto ainda não abordado nas declarações da empresa: as células T. Os anticorpos são apenas uma parte da resposta imune. As células T são outra. Ambos podem formar proteção duradoura por conta própria, mas as células T ajudam na manifestação de anticorpos. Isso é importante porque as vacinas de DNA e RNAm são mais eficazes em acionar células T, diz Bottazzi, mas avaliar essa resposta é difícil e normalmente isso é reservado para fases posteriores de estudos em humanos.
Ainda assim, a Moderna pode ter um longo caminho pela frente. Os participantes da fase dois devem ser monitorados por pelo menos 15 meses. Contudo se os primeiros sinais forem positivos, o candidato à vacina poderia chegar aos estágios finais ainda este ano.
Independentemente do sucesso da Moderna, o mundo precisará de diversas versões para vencer a pandemia. Globalmente, mais de cem estudos com candidatos à vacina contra a covid-19 estão em andamento e, até agora, diversas empresas estão relatando resultados promissores revisados por pares. Ter um grande número de possibilidades é vantajoso porque se um candidato à vacina falhar, os outros poderão continuar oferecendo esperança, afirma Bottazzi.